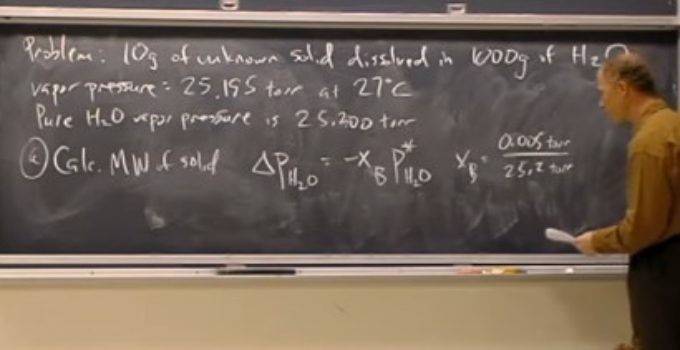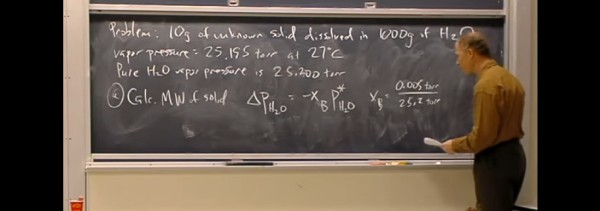Lama tóxica


No dia 4 de outubro de 2010 ocorreu um trágico acidente na Hungria, com o vazamento de uma grande quantidade de resíduos do processamento da bauxita, causando a morte de 10 pessoas.
A lama de cor avermelhada é uma mistura de compostos resultantes do Processo Bayer empregado na purificação da bauxita para obtenção de alumina (óxido de alumínio (Al2O3). Esta lama portanto contém as impurezas da bauxita, com presença de titânio, vanádio e óxido de ferro, que confere a cor avermelhada. Algumas fontes alegaram que o material continha também quantidades perigosas de metais pesados, mas tal informação foi negada pela Academia de Ciências da Hungria.
O perigo desta lama estava na sua elevada alcalinidade, apresentando um pH em torno de 13. Isto devido à presença de hidróxido de sódio no resíduo do processo. E por ter chegado a um afluente do Rio Danúbio, resultando em danos significativos para a ecologia da região.
Assista no vídeo abaixo os comentário do Professor Martyn Poliakoff sobre este trágico evento.
Vídeo com legendas em português. Ative pelo botão CC que aparecerá no vídeo.
ATUALIZAÇÃO: O lama deste acidente na Hungria não tem necessariamente a mesma composição e perigo da lama do acidente ocorrido em Bento Rodrigues (MG) em 05 de novembro de 2015.
Texto escrito por Prof. Dr. Luís Roberto Brudna Holzle.