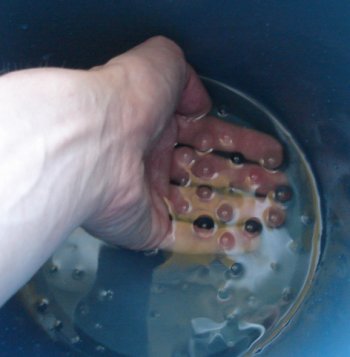
Fósforo – branco, vermelho e preto


O fósforo existe em diferentes formas alotrópicas.
O fósforo branco é P4 e reage fortemente com o oxigênio do ar resultando em um intensa luz branca. Por isso é armazenado em água para evitar a reação.
O fósforo é um elemento muito importante em nosso corpo. Uma pessoa de tamanh médio contém em média 500 gramas de fósforo.
Veja no vídeo abaixo mais informações e demonstração da reação de fósforo com ar.
O vídeo foi legendado em português. Para ver a legenda, clique no PLAY e depois ative a legenda clicando no botão no inferior direito e selecione “Ativar Legendas >> Português”.
Texto escrito por Prof. Dr. Luís Roberto Brudna Holzle ( luisbrudna@gmail.com ) – Universidade Federal do Pampa – Bagé.